領域概要
Overview
バイオロジカルクラスターとは?
生き物の細胞内では、多種多様なタンパク質が様々な機能を発揮することで生命活動が維持されています。
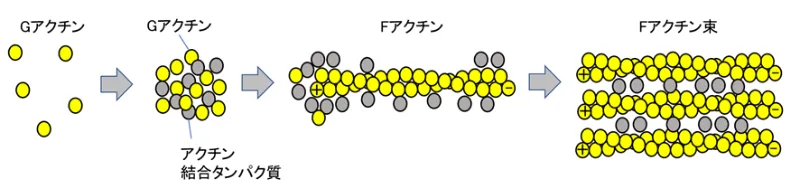
タンパク質の中には、いくつかが集まって複合体をつくり、さらにそれらの複合体が集まってクラスターをつくることで、全体として機能を発揮するものがあります。
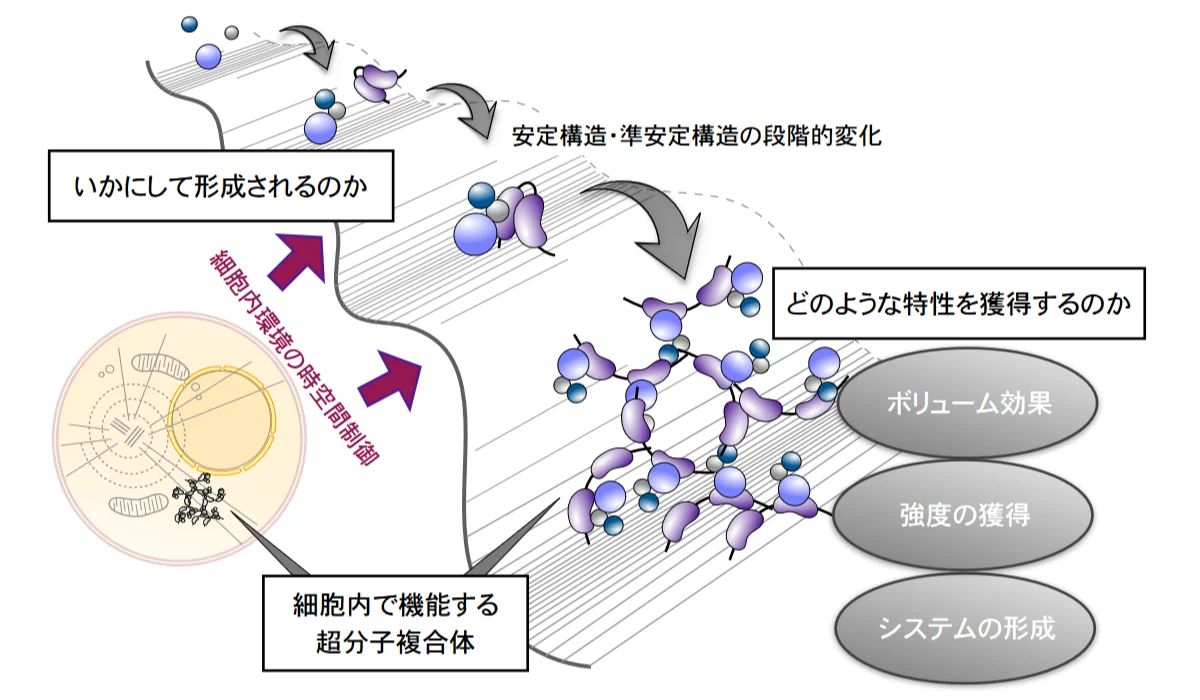
本研究領域では、クラスターを形成することで生物学的な意義を発揮する、こうした超分子複合体を「バイオロジカルクラスター」と定義し、形成のメカニズムや、発揮される機能の特性を解明する研究を行います。
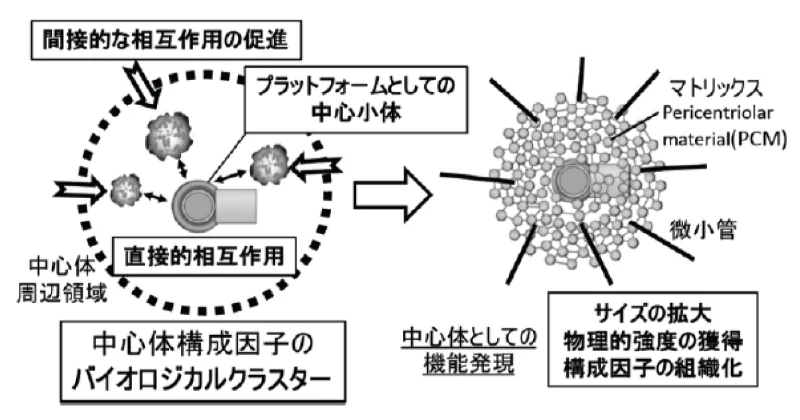
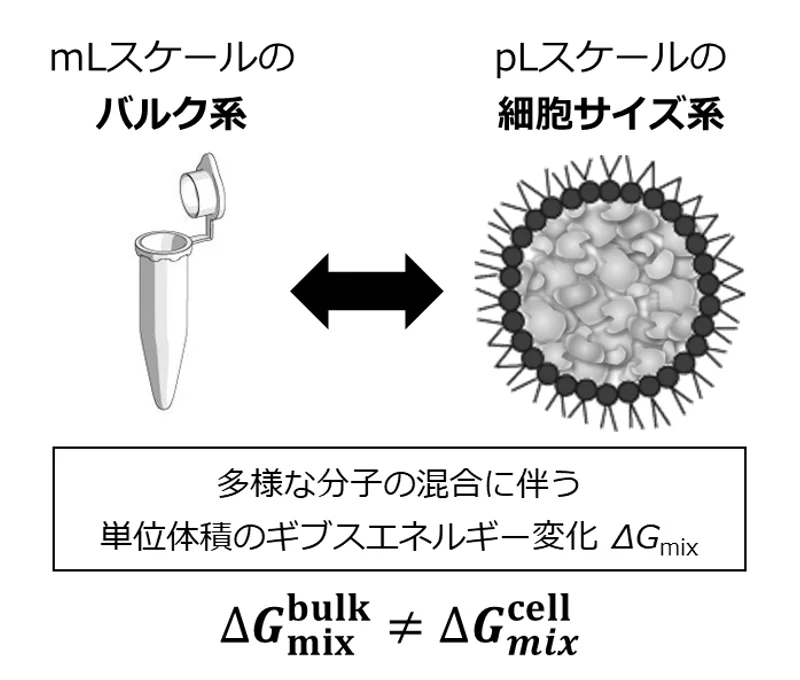
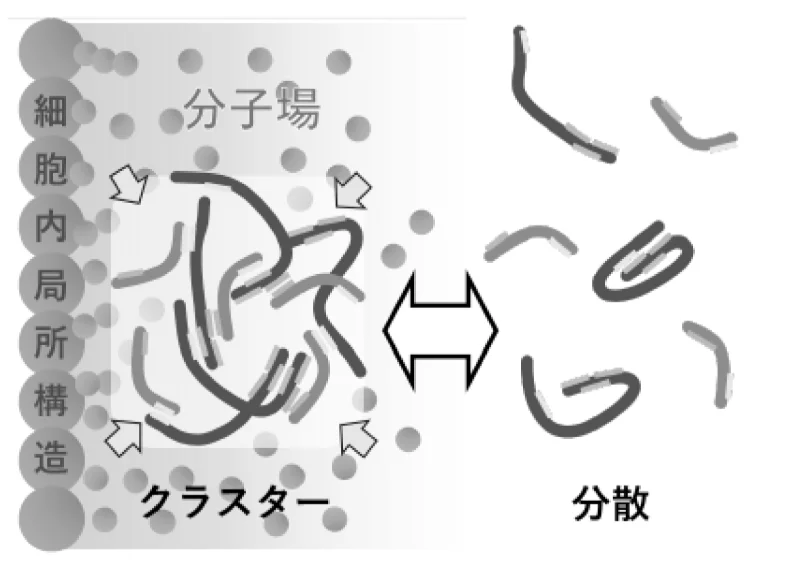
例えば、細胞内でクラスターを形成することにより、一定の体積を確保し、物理的な強度を獲得して、機能的なシステムを形成することで、統御された超分子複合体として機能するものが存在しています。
さらに、細胞内でのクラスター形成には、分子間相互作用に加え、分子混雑環境の空間効果やプラットフォーム効果など様々な要因が関与する可能性が考えられます。
これらを考慮し、蓄積されつつあるタンパク質複合体の構造情報と細胞内の超分子複合体との間のギャップを埋める、「バイオロジカルクラスター」研究は、生物学に転換を促す挑戦と言えます。
本研究領域のアプローチ
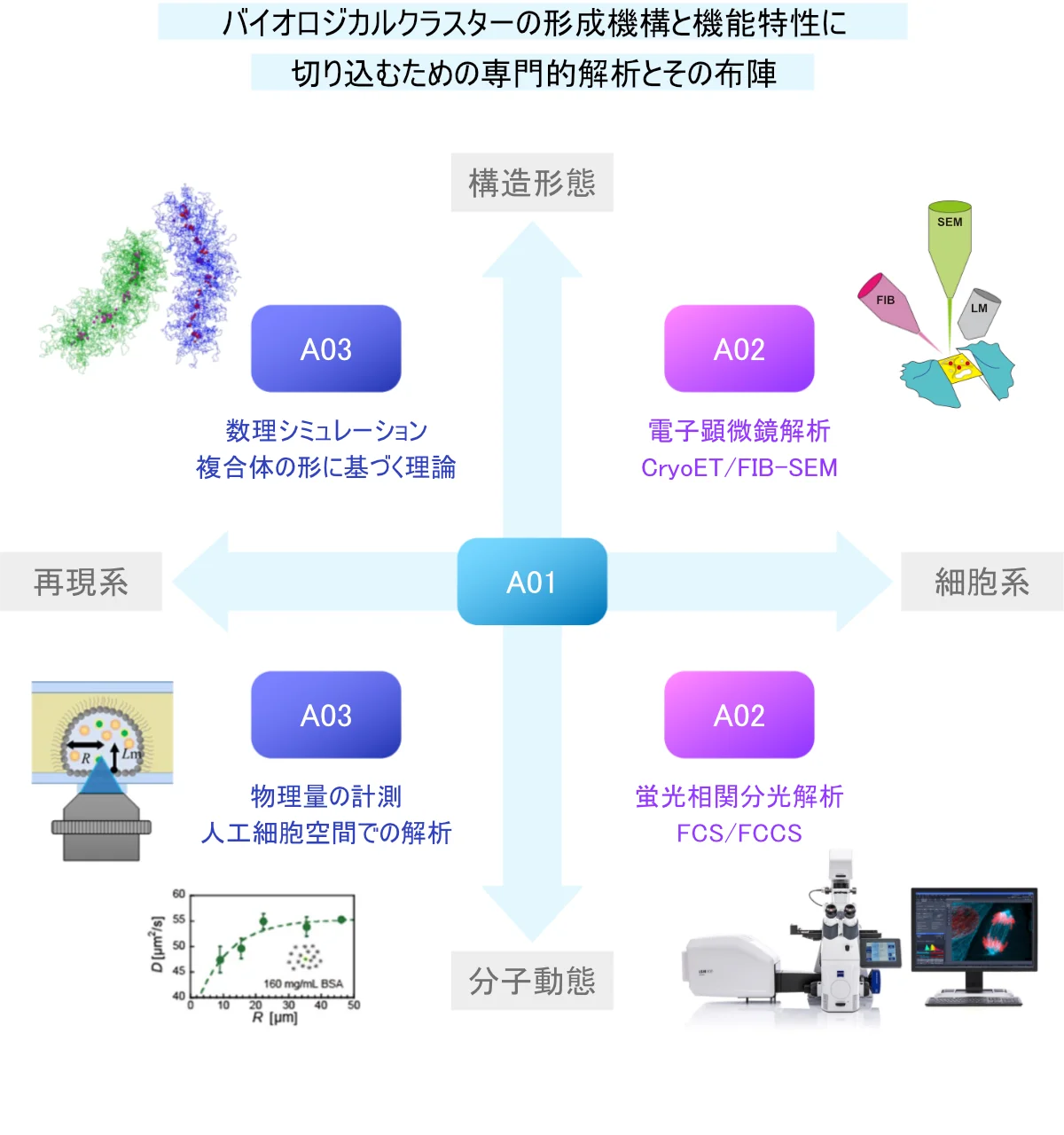
バイオロジカルクラスターの成り立ちとその意義を解析するには、既存の細胞生物学・生化学・構造生物学に加えて、先進的な電子顕微鏡、蛍光相関分光法、超解像イメージング法を駆使した解析、さらには、その動態を物理学的に取り扱う、いわゆるソフトマター物理学や数理シミュレーション等を融合させる必要があります。細胞内で観察された現象や測定された物理量に対して物理学の理論を持ち込むことで理解を深め、生物学と物理学を相互に補完していくというこれまでにない融合研究を推進します。
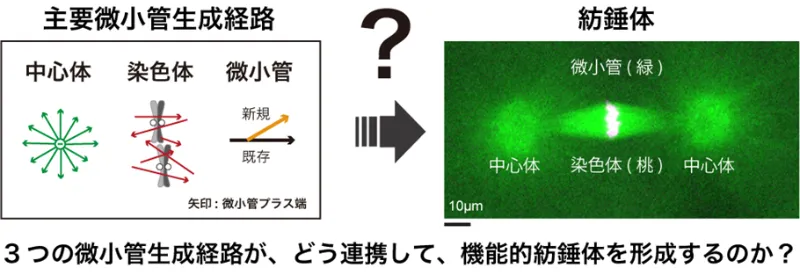
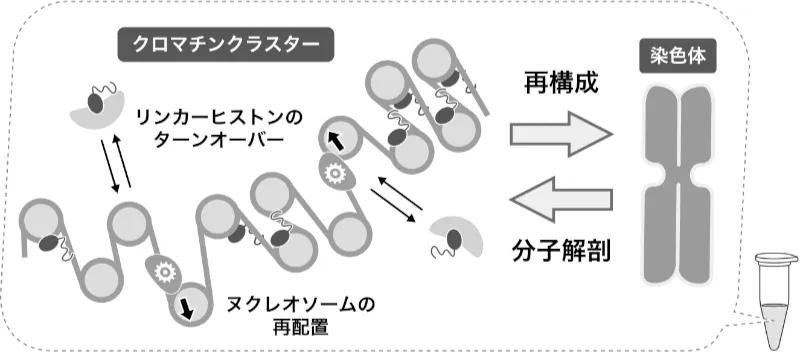
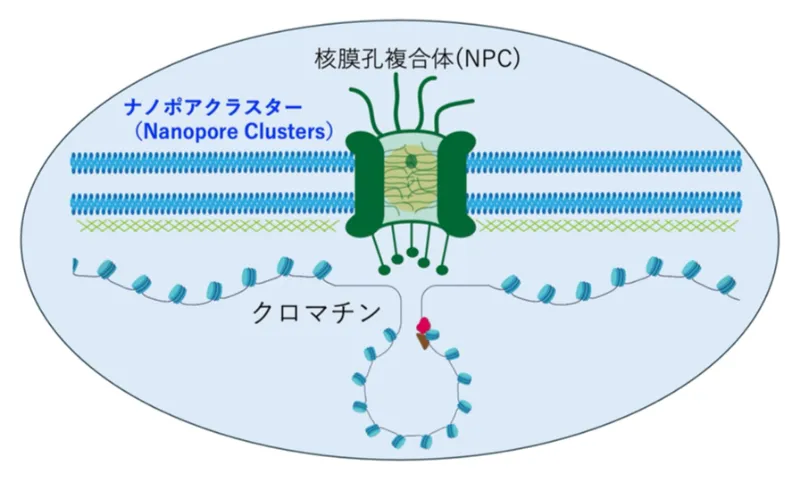
本領域では特に、中心体、セントロメア、染色体など、細胞内に存在する超分子複合体を対象とし、その構造基盤や形成原理の解明を目指します。
研究項目
A01バイオロジカルクラスターの分子基盤と細胞内機能との関連解明
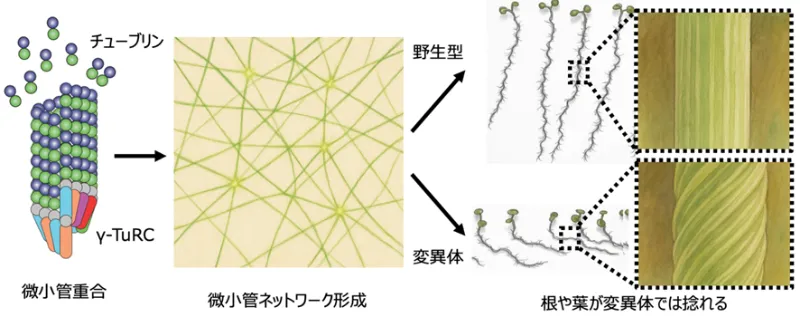
各超分子複合体を対象に、クラスター形成に関わる要因を見出し、細胞内でのクラスター化の実体とその形成制御、クラスター化することで獲得する特性を解明することによって、それらがどのように特異的な細胞内機能と関わるのかを理解することを目指します。
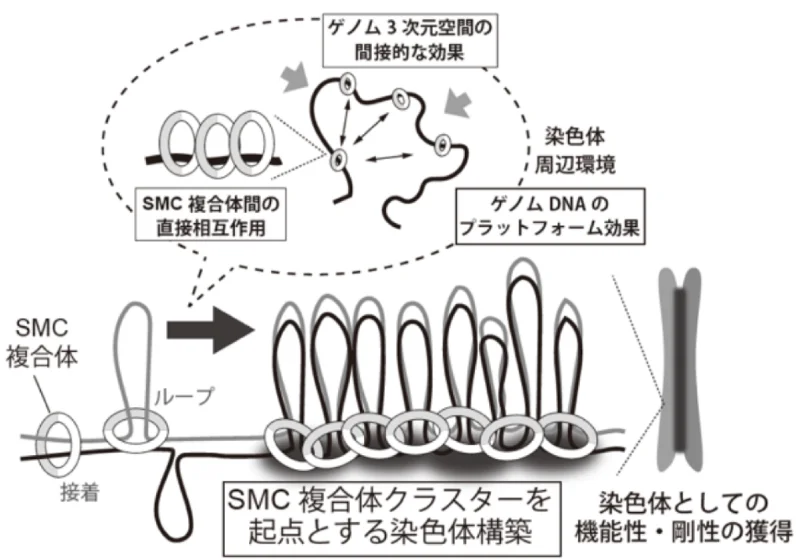
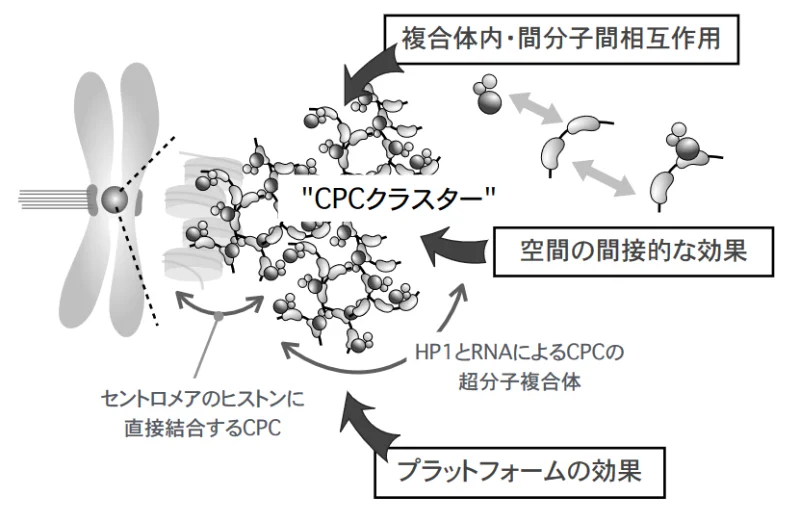
具体的に計画班では、動原体複合体、染色体を構成するSMC複合体、セントロメアを制御するCPC複合体、中心体を構成する各種複合体について、基本ユニットの構造・生化学的な解析、変異体細胞や人為的クラスター誘導細胞の実験系を用いた細胞生物学的解析を行います。得られた知見をA02、A03班と共同で解析することで、これらの複合体が細胞内でクラスターを形成する機構とそれによって得られた特性を解明して、細胞内機能との関連を理解します。
計画班
公募班
Architecture, Regulation and Performance of Mitotic Stress Memory
代表者:Franz Meitinger(Assistant Professor, Okinawa Institute of Science and Technology)
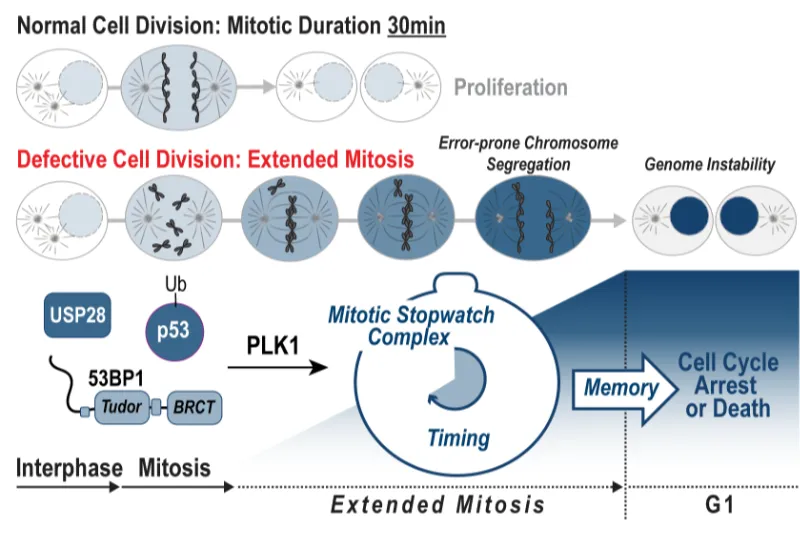
Mitotic defects drive genome instability, a hallmark of cancer. Cells counter this by assembling a mitotic stopwatch complex that senses prolonged mitosis caused by mitotic stress and halts proliferation of the daughter cell. This project will define the complex’s structure and uncover how it measures mitotic duration and encodes a heritable memory of mitotic defects.
研究項目
A02バイオロジカルクラスターの可視化と分子動態制御基盤の解明
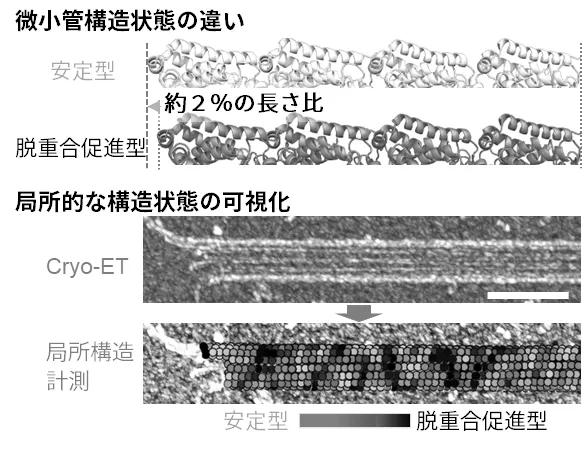
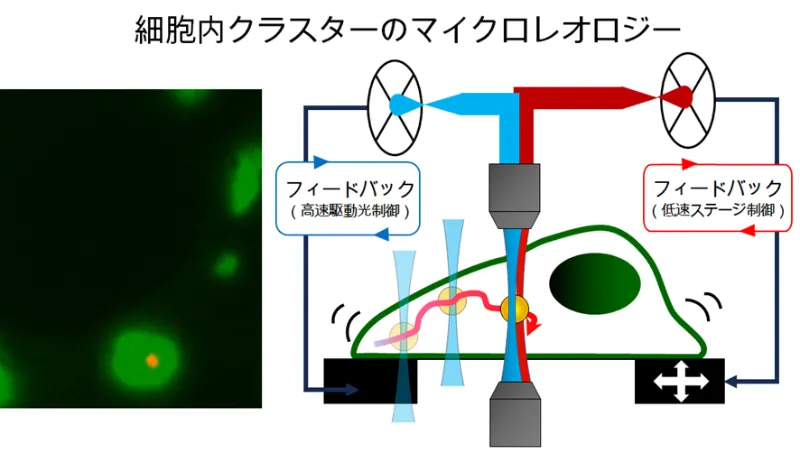
先進的な電子顕微鏡や超解像イメージングにより、細胞内でのクラスターの制御と構造の特性を明らかにし、分子動態解析により各クラスターの体積や強度といった「物理的特性」とシステム形成のような「生化学的特性」の分子動態制御基盤を解明します。
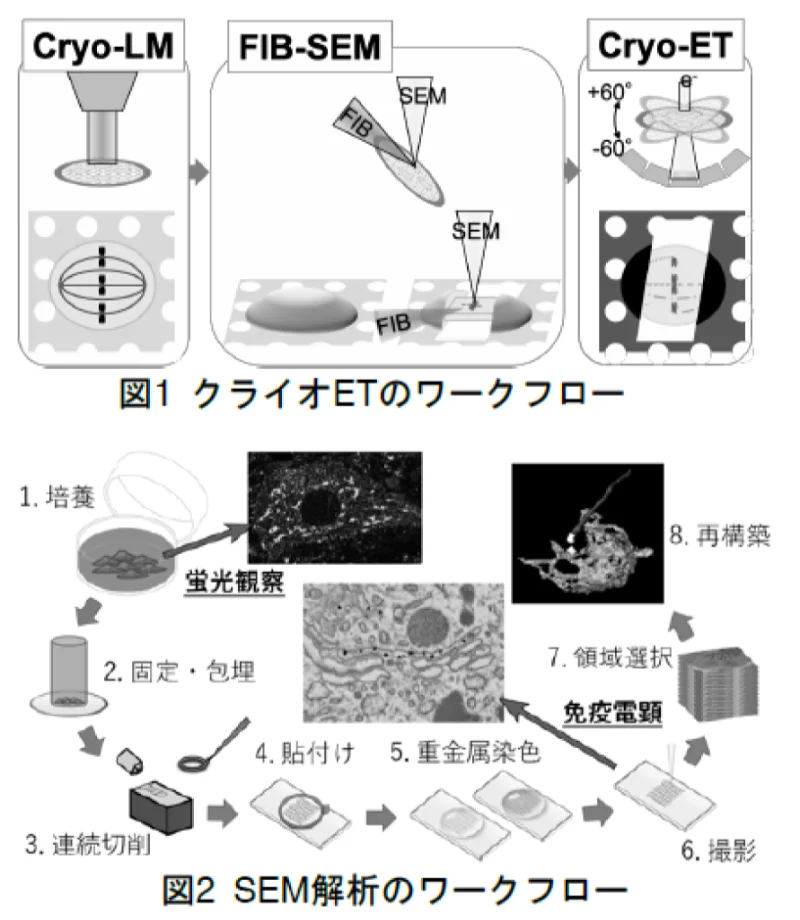
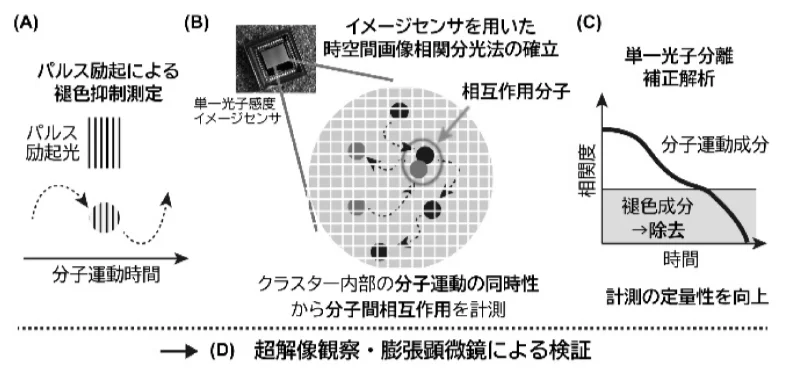
具体的には、A01で扱う各複合体の細胞内での高次クラスター化の実体や特性をクライオET、超解像顕微鏡、エクスパンジョン顕微鏡といった先進的イメージング技術を駆使して解析します。その際A01の研究で明らかにする複合体の相互作用データをレファレンスとして活用します。また、従来からの蛍光相関分光法(FCS、FCCS)に加えて、新しい極限時空間相関分光法を確立し、バイオロジカルクラスターの細胞内での特性や動態の定量的解析を行います。
計画班
公募班
研究項目
A03物理・理論的解析によるバイオロジカルクラスターの形成と特性の解明
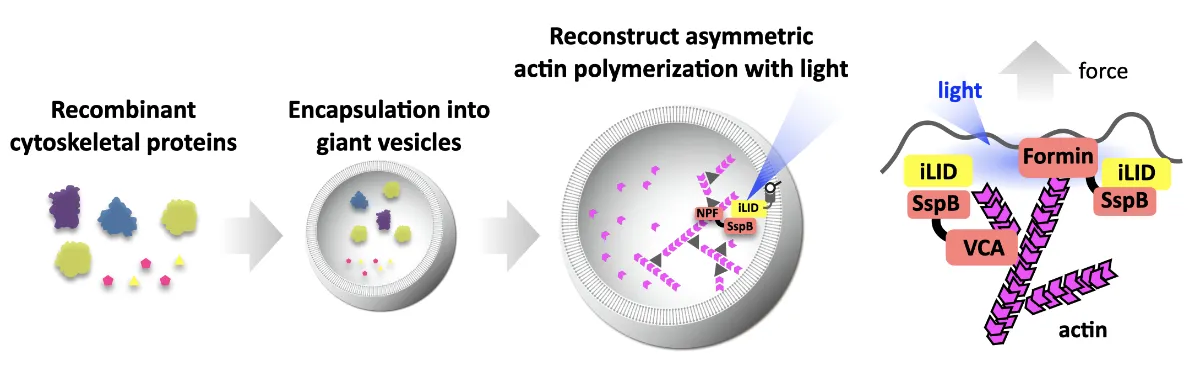
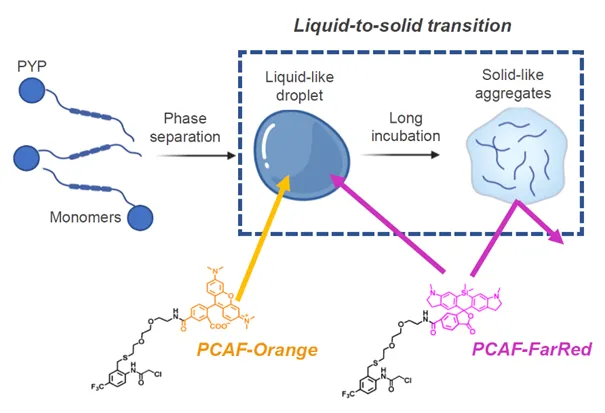
人工細胞系を用いることで、細胞サイズの空間でのクラスター形成と獲得特性に関わる物理量を測定し、A01、A02から見出される細胞内の動態解析データとも比較しつつ、数理理論解析と相互補完することでクラスターに作用する直接的・間接的な要素を解明します。
具体的には、領域で扱う超分子複合体を各種設計した人工細胞に導入し、そこで形成した各クラスターの物理量を測定することで、細胞サイズ空間がつくる間接的な効果やプラットフォーム(場)は何かを明らかにします。また、ここで得られた知見とA01、A02での実験結果を取り込んで、クラスター形成過程の数理シミュレーションを行います。それをA01、A02の研究に再フィードバックして、実験的検証を行い、その精度を高めていきます。